Mykoplasmen-Nachweis, Prävention und Eliminierung Praxis - Inhouse Schulung
Inhalte & LernzieleKontaminationen sind nach wie vor ein immer wieder auftretenden Problem in der Zellkultur. Mykoplasmen im speziellen stellen derzeit - noch vor Kreuzkontaminationen - das größte Problem in der zellbiologischen Wissenschaft und industriellen Verwendung von Zellkulturen als Testsystem oder Produktionssubstrat dar. Selbst unter GMP ist davon auszugehen, dass 4-5% aller Zell-Linien mit Mykoplasmen kontaminiert sind; in der Forschung je nach Labor 15 bis 80%. Dies begründet sich vor allen darin, dass Mykoplasmen im Mikroskop nicht erkennbar sind sondern eine spezifische Detektion erfordern. Dieser Kurs vermittelt Ihnen die notwendigen Kenntnisse, um Kontaminationen durch Bakterien und Mykoplasmen in der Zellkultur frühzeitig zu erkennen und zu unterscheiden. Wir stellen Ihnen einfache und praktikable Verfahren zur Prävention in der täglichen Routinearbeit, zum Nachweis mittels verschiedener Kits und Methoden am Markt und zur Eliminierung vor. |
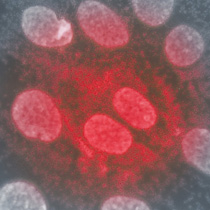 |
Neben den Auswirkungen auf die wissenschaftliche oder industrielle Arbeit werden Kontaminationswege und Hygienemaßnahmen beschrieben. Ferner werden Verfahren zur Entfernung von Mykoplasmen aus Kulturen vorgestellt und diskutiert. Im Praxisteil werden Mykoplasmen mit zwei Nachweis-Kits nachgewiesen und die Durchführung vergleichen.
Themen des Theorie-Seminars
|
|
Themen der Praxis-Schulung
|
Die Versuchsergebnisse, mögliche Fehlerquellen bei der Assay-Durchführung und deren Vermeidung werden während des Kurses besprochen.
Erweiterungsthemen bei In-house Schulungen
Diese Inhalte werden bei In-house Kursen je nach Bedarf und Kundenwunsch angepasst, ergänzt und gekürzt. Weitere Themen könnten z.B. sein
- Aseptik und Hygiene
- Zellkultur Qualitätsmanagement
- Mykoplasmen
- GMP für ATMP
- GMP Grundlagen
- SOP Grundlagen
- Bioassays
Vorab schon interessant sind evt. folgende Seiten:
- Infoseite Zellkultur Kontaminationen
- Infoseite Mykoplasmen
- Infoseite Mykoplasmentests
- Ein sehr unterhaltsames Video zur Durchführung eines Mykoplasmentests mittels PCR (aus einem DNA MOOC, produziert von Frau Dr. Kühl)
Zielgruppe
In-house: Dieser Kurs ist 1-tägig angelegt, wird jedoch je nach Kundenvorgabe oft auf 2 Tage ausgeweitet und mit weiteren Themen aus dem Bereich Kontaminationen sowie Aseptik und Hygiene kombiniert. Ihre besonderen Wünsche und Anforderungen besprechen wir vorab in einem zwanglosen und unverbindlichen Telefonat. Unsere Kontaktdaten finden Sie hier.
Termine und Preise
Für In-house Schulungen kontaktieren sie uns gerne per mail oder telefonisch, dann erstellen wir Ihnen ein individuelles Angebot, das sich nach den Inhalten und der Dauer des In-house Kurses richtet. Bereits ab 4-5 Teilnehmern ist ein In-house-Kurs günstiger als die individuelle Schulung ihrer Mitarbeiter durch Teilnahme an offenen Fortbildungen. Den Termin der Schulung sprechen wir natürlich mit Ihnen ab. Generell kann ein Kurs innerhalb von 4-8 Wochen nach dem Erstkontakt bei Ihnen durchgeführt werden. Ihre besonderen Wünsche und Anforderungen besprechen wir vorab in einem zwanglosen und unverbindlichen Telefonat. Unsere Kontaktdaten finden Sie hier.
Die Kursgebühr bei In-house Schulungen beinhaltet die Schulungsunterlagen im Farbdruck, ein Teilnahme-Zertifikat sowie die Reise- und Hotelkosten der Dozentin oder des Dozenten.
Vorteile von In-house Schulungen
- Ab 4-5 Teilnehmern ist eine In-house Schulung günstiger
- Ihre Mitarbeiter müssen nicht reisen
- Das Trainingskonzept wird individuell für sie zusammengestellt und an Ihre Ziele und Mitarbeiter angepasst
- In Praxisschulungen kann Ihr Assay im Kurs durchgeführt werden, dies hilft beim trouble shooting
- Alle Mitarbeiter Ihrer Abteilung sind an der Entwicklung neuer Standards aktiv beteiligt. Dies erhöht die Compliance
- Die Praxisteile finden in Ihren Laboren statt und alle Ergebnisse sind direkt übertragbar
- Optimierungsvorschläge sind so auch bei Räumen und Abläufen möglich
Kursstruktur und Planung:
- Kursbeginn (am ersten Tag) 09:00 Uhr
- Kursende (bei eintägigen Kursen) ca. 17:00
- Kursende (bei mehrtägigen Kursen bis zum vorletzten Tag) ca. 17:00 Uhr
- Kursende (bei mehrtägigen Kursen am letzten Tag) ca. 16:00 Uhr
Ort des Trainings
Diesen Kurs führen wir gerne in ihren Räumen durch.
- In-house Kurse: wir kommen zu Ihnen - die Wahl für mehrere Personen aus einem Unternehmen
Trainingsarten: Theorie und Praxis
Um ein effektives Lernen zu fördern, versuchen wir immer Theorieteile und Praxisteile in einem Kurs miteinander zu kombinieren. So kann das neu Erlernte im Labor direkt in die Praxis umgesetzt werden. Feed-back und praktische Übungen helfen dabei, den Lernerfolg zu vertiefen und direkt in Abläufe zu integrieren. Wenn sie jedoch Ihren Mitarbeitern und Kollegen schnell einen Überblick über viele Themen geben wollen, können diese Themen auch in einem Theorie-Seminar interaktiv bearbeitet werden.
- Theorie: Offener Kurs und In-house Schulungen
- Praxis: Offener Kurs und In-house Schulungen
Dozent
Dozentin
| Dr. Nicole Kühl hat an der TU Karlsruhe und der Universität Bremen Biologie studiert. Sie promovierte 1999 als Zell- und Molekularbiologin über Zellzyklus und Hitzeschockproteine. Danach wechselte sie an das Akademische Krankenhaus Groningen, Niederlande. Dort spezialisierte sie sich auf therapieorientierte Multiple Sklerose-Forschung und begann mit primären Gliazellen zu arbeiten. Dies setzte sie an der Jacobs University Bremen fort, wo sie ab 2003 eine Arbeitsgruppe hatte und als Dozentin „Biochemistry and Cell Biology“ unterrichtete. Von 2008 bis 2011 war Dr. Nicole Kühl die Leiterin der PromoCell Academy in Heidelberg und Dozentin für Zellkultur- und QM Kurse. Seit 2012 ist sie als selbstständige Dozentin und Beraterin im Bereich Zellkultur QM und GMP tätig und betreibt das Trainings-Portal www.InCelligence.de. Sie berät pharmazeutische Unternehmen und Hersteller von Inkubatoren, Zellzählgeräten und Verbrauchsmaterialien. Seit 2016 ist Dr. Kühl external Head of QA der ANOVA IRM GmbH. Dort hat sie eine Herstellerlaubnis nach §13 AMG sowie eine Erlaubnis nach § 20b, c AMG für 2 stammzell-basierte Arzneimittel (BMC und Sekretom aus mesenchymalen Stammzellen, RPDA 2018) erwirkt. Dr. Kühl war Mitglied im DIN Arbeitskreis Biorektoren für das Tissue Engineering. Lernen Sie sie in einem MOOC Video kennen. |  |


