Zellkultur-CO2-Inkubatoren: Übersicht und Vergleich
Was soll ein Inkubator können oder mitbringen?
Natürlich soll ein Inkubator in der Zellkultur die Temperatur, Luftfeuchte und den CO2-Gehalt regeln.
Aber ist das schon alles ? Nein!
Es gibt viele Dinge, die man sich genauer ansehen sollte, ganz besonders dann, wenn man einen neuen Brutschrank kaufen möchte. Unsere Übersicht über die Kriterien und der Vergleich verschiedener Hersteller soll ihnen hierbei helfen: Zu den wichtigsten Kriterien gehören:
|
|
Welchen Stellenwert man den einzelnen Punkten bei der Kaufentscheidung einräumt, hängt auch davon ab, ob man in einem Forschungslabor arbeitet, in einem Testlabor oder ob man z.B. ein ATMP (advanced therapy medicinal product) oder TEMP (tissue engineered medicinal product) herstellen möchte. Eine Gewichtung der Kaufkriterien, die man unserer Meinung nach beim Vergleich der Hersteller berücksichtigen sollte, findet sich ganz am Ende dieser Seite.
Temperaturkonstanz und Erholung nach Türöffnung
Prinzip der Beheizung im Brutschrank
|
Für Inkubatoren in der Zellkultur gibt es zwei wichtige Prinzipien, wie die Temperaturkonstanz hauptsächlich gewährleistet wird: + Wassermantel-Inkubatoren Vorteile: bessere Temperaturkonstanz, weniger hohe Schwankungen bei Türöffnung, längere Temperaturhaltezeit bei Stromausfall Nachteile: der Inkubator wird schwerer und ist damit schwerer zu bewegen, langsamere Temperaturerholung bei langen Öffnungen, Wartung beinhaltet den Wasseraustausch - Luftmantel-Inkubatoren Vorteile: der Inkubator ist leichter und ist dadurch leichter zu bewegen, schnellere Temperaturerholung bei langen Öffnungen, Wartung ohne Wasseraustausch. Höhere Desinfektions- und Sterilisationstemperaturen sind möglich. Nachteile: schlechtere Temperaturkonstanz, größere Schwankungen bei Türöffnung, kürzere Temperaturhaltezeit bei Stromausfall. Bei manchen modernen Inkubatoren wird dies durch eine schnellere Messung und bessere Steuerung ausgeglichen. |
|
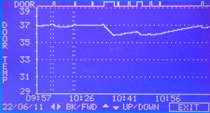
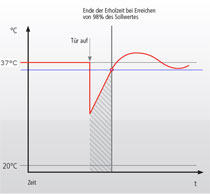
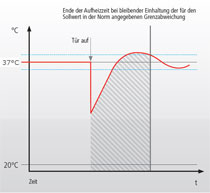
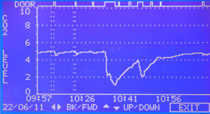
Messung der Erholung nach TüröffnungDer Vergleich von Inkubator-Herstellern kann über die Angaben zu den vorgeschriebenen DIN Prüfung erfolgen (Baumusterprüfung). Daten hierzu findet man normalerweise in den Gerätespezifikationen auf der Website, den technischen Informationen der Betriebsanweisung oder man lässt sie sich zuschicken. Die Erholungszeiten der Temperatur werden normalerweise gemäß der DIN Norm für Inkubatoren gemessen und dann in Minuten angegeben. Hier muss man wissen, dass die DIN 12880 Reihe im Jahr 2007 geändert und aktualisiert wurde. Die neue Version heißt DIN 12880:2007-05. Wichtig hieran ist, dass die Messverfahren für die Erholung nach Türöffnung maßgeblich geändert wurden und daher Messungen nach den neuen Vorgaben längere Erholungszeiten ausgeben. Außerdem sind nun in größeren Brutschränken wie in der Zellkultur 27 statt 9 Messpunkten vorgeschrieben, die Messungen sind also präziser. Die Messung nach der alten und neuen DIN Norm sind in den Bildern rechts (oben bzw. unten) dargestellt. Nach der alten Norm ist die Temperaturerholung nach 30s Türöffnung dann erreicht, wenn der Inkubator erstmals über die untere Temperaturtoleranzschwelle ansteigt. Hierdurch wird eine vermeintlich schnelle Erholung erreicht. Nach der neuen DIN Norm ist die Erholung nach 15s Türöffnung jedoch erst dann erreicht, wenn die Temperatur den Toleranzbereich nicht mehr verlässt. D.h. die Türöffnung wurde verkürzt, aber die Erholung ist strikter geregelt. Dies bedeutet, dass man Messung nach der alten und der neuen Norm nicht direkt miteinander vergleichen kann. Darüber hinaus sollte man darauf achten, dass der Inkubator eine separate Heizung für die Tür hat (also alle 6 Seiten beheizt sind), damit dort kein Wasser kondensiert und kein Temperaturgradient entsteht. Im Vergleich zum Abfall des CO2-Gehalts bei Türöffnung ist die Verringerung der Temperatur jedoch eher ein weniger wichtiges Kriterium. |
|
Temperaturbereiche von Brutschränken
Neben diesen Punkten sollte man noch darauf achten in welchem Temperaturbereich der Umgebung die Brutschränke arbeiten können. Zellkultur-Inkubatoren heißen nämlich auch Brutschränke, weil sie nur wärmen, aber im Normalfall nicht aktiv kühlen können. D.h. ein normaler Brutschrank benötigt eine Temperaturdifferenz von ca. 5-7 Grad zur Raumluft. In Laboren ohne Klimaanlage kann dies im Sommer durchaus ein kritischer Faktor sein, da durch Sonneneinstrahlung auf den Inkubator oder große Fenster im Labor an bestimmten Stellen im Labor Temperaturen deutlich erhöht sein können.
Das Prinzip der Befeuchtung
Damit während der Kultur der Zellen im Inkubator aus den Kulturschalen, -flaschen und Multiwells keine Flüssigkeit verdunstet, muss der Innenraum des Inkubators ca. 95 % Luftfeuchte aufweisen. Ansonsten werden die Zellen zwischen den Medienwechseln einem kontinuierlich zunehmenden osmotischen Stress ausgesetzt. Einen Vergleich der generellen Wege um den Inkubator-Innenraum effizient zu befeuchten, haben wir hier aufgeführt. Beim Inkubatorkauf ist wichtig, die Erholzeit nach Türöffnung zu erfragen und zu vergleichen. Bei alten Modellen kann eine lange Türöffnung Schwankungen bis zu 8 h nach sich ziehen.
|
- Direkte Wasserbefüllung des Inkubator-Bodenraums (unseres Erachtens ein "no-go") + günstiger als die anderen Varianten |
|
|
+ Indirekte Befeuchtung durch eine Wasserwanne im Inkubator (Stand der Technik) + günstiger als Verdampfungsvariante |
|
|
+ Befeuchtung durch aktive Verdampfung von Wasser (Vorsicht Systeme vergleichen) + sicherste Variante, |
CO2-Gehalt und die Erholungszeit nach Türöffnung
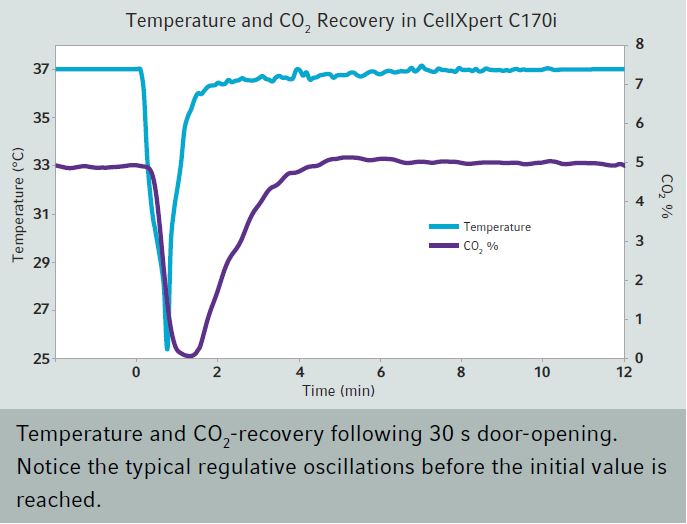
Für das Wachstum der Zellen im Zellkultur-Inkubator ist dieser Faktor derjenige über den man am meisten nachdenken sollte. Zum einen sollte der Inkubator den CO2-Gehalt möglichst konstant halten und zum anderen sollte man dafür sorgen, dass möglichst wenig CO2 verloren geht, indem man die Türen so kurz und so selten wie möglich öffnet. Geteilte und gut dichtende Türen sind hierbei ebenfalls wichtig (s.u.).
Die Regelung des pH-Werts im Medium
|
Der CO2-Gehalt im Inkubator sorgt dafür, dass im Zellkulturmedium der richtige pH-Wert eingestellt wird. Es besteht ein Gleichgewicht zwischen der Menge an Natriumhydrogencarbonat im Medium und CO2-Gehalt der Luft im Inkubator. Je höher der CO2-Gehalt, desto niedriger der pH-Wert. Gängige CO2-Gehalte für Zellkultur-Inkubatoren sind 5%, 8,4% oder 10%, je nach Medium das verwendet wird. Im Verlauf der Kultur wird das Medium durch die sauren Abfallprodukte, die die Zellen ins Medium abgeben immer saurer. Wenn sich das Medium orange verfärbt hat, sollte meist ein Mediumwechsel vorgenommen werden, damit der pH-Wert nicht in unphysiologische Bereiche abfällt. |
|
Messprinzip des CO2-Gehalts |
|
|
Der CO2-Gehalt kann im Brutschrank über zwei Verfahren gemessen werden: TC (thermal conductivity) und IR (Infrarot) Sensoren. Heute sollte man nur noch Zellkultur-Inkubatoren mit dem schnelleren Infrarot-Messprinzip kaufen und darauf achten, dass es ein guter Sensor ist (Messzeit und Genauigkeit). TC Sensoren werden durch Schwankungen der Temperatur und Feuchte, die bei Türöffnungen entstehen, beeinflusst und sind deshalb im Vergleich langsamer und zeigen nicht die realen Werte in Echtzeit an. D.h. das Display sagt zwar: 5%, aber der reale Wert kann auch deutlich darunter liegen. Bei älteren Modellen mit TC Sensor ist die Erholungszeit daher zu lang und damit die pH-Wert Verschiebung für die Zellen größer bzw. länger. IR Sensoren dagegen reagieren im Vergleich schneller, da hier eine direkte Messung der der CO2 Konzentration (unabhängig von den Umgebungsbedingungen: Temperatur und Luftfeuchtigkeit) erfolgt, sie zeigen Echtzeitwerte und sorgen damit auch für eine schnellere Erholung und eine präzisere Regulation des CO2-Gehalts. Außerdem gibt es Sensoren, die man im Brutschrank belassen kann während man ihn hitzedekontaminiert während man ältere Sensoren vor der Sterilisation ausbauen muss. Ersteres ist natürlich bequemer und schneller. |
 |
Konstanz des CO2-Gehalts bei der Kultivierung |
|
|
Die Konstanz und die Erholungszeiten des CO2-Gehalts werden normalerweise gemäß der DIN Norm für Inkubatoren gemessen und dann in Minuten angegeben. Hier muss man wissen, dass die DIN 12880 Reihe im Jahr 2007 geändert und aktualisiert wurde. Die neue Version heißt DIN 12880:2007-05. Wichtig hieran ist, dass die Messverfahren für die Erholung nach Türöffnung maßgeblich geändert wurden und daher beim Vergleich Messungen nach den neuen Vorgaben längere Erholungszeiten ausgeben. Diese Zeiten muss man unbedingt beim Hersteller erfragen, wenn man Inkubatoren vergleichen möchte. |
 |
Anzahl der Türen zur Schwankungsminimierung
|
Bei jeder Türöffnung entweicht CO2 und warme Luft. Je länger die Türöffnung anhält oder je größer die offene Fläche ist, desto größer wird die Schwankung im Inkubator. Dies stellt besonders dann ein Problem dar, wenn viele Personen sich einen Inkubator teilen, also die Türen häufig geöffnet werden. Andrerseits verliert der Brutschrank Gas durch die Dichtungen, auch wenn keine Türen geöffnet werden (vgl. Dichtigkeit der Türen). Daher ist es prinzipiell immer vorzuziehen, eine unterteilte Tür zu kaufen, wenn viele Personen einen Inkubator nutzen, außer man arbeitet mit Hypoxie (s.u.). Die geteilte Tür ist meist deutlich teurer, lohnt sich aber, weil die Konstanz zu besserer Vergleichbarkeit der Ergebnisse beiträgt. Diese Investition sollte man dann immer tätigen! Je nach Hersteller und Model gibt es Brutschranktüren ungeteilt, mit 2, 3, 4, 6 oder 8 Türen. Allerdings schränken die Türen die Beladungsmöglichkeiten ein. Daher können 4 Türen unter beiden Gesichtspunkten durchaus besser sein als 6 oder 8 Türen. Das Bild zeigt den alten New Brunswick Inkubator, der jetzt mit neuem Design (s.u.) von Eppendorf hergestellt wird. |
 |
Dichtigkeit der Türen
|
Ein Punkt bei dem man laufende Kosten verringern kann, ist die Dichtigkeit der Türen. Man sollte darauf achten, wie die Türenscharniere angebracht sind und wie leicht man sie beim Öffnen nach unten oder oben drücken kann. Im Gegensatz zum oberen Bild kann man hier sehen, dass die Scharniere über die gesamte Höhe der Tür gehen und mehrfach verschraubt sind. So sieht das hochwertige Scharnier des neuen Eppendorf Galaxy Inkubators (vorher New Brunswick) aus! Darüber hinaus sind Türen dichter, je weniger Unterteilungen es gibt. Dies ist besonders wichtig bei Inkubatoren, die mit Hypoxie gefahren werden. Für diese muss man genau überlegen, ob man geteilte Türen kaufen sollte. Eine beispielhafte Darstellung gibt die Tabelle für einige Binder Inkubatoren. Bei anderen Inkubatoren gilt jedoch analog das gleiche Prinzip. |
 |
Gasverbrauch pro Tag und pro Türöffnung im Vergleich für Binder Inkubatoren
|
CB 150/ CB 170 |
Standard- |
Geteilte |
Break- |
|
CB 210/ CB 220 |
|
Standard- |
Geteilte |
Break- |
|
|
Sollwert |
Gasverbrauch |
g |
g |
|
Sollwert |
Gasverbrauch |
g |
g |
|
|
|
5 % CO2 |
CO2 pro Tag |
0,7 |
2,7 |
|
5 % CO2 |
CO2 pro Tag |
1,0 |
5,0 |
|
|
|
|
CO2 pro Türöffnung |
13 |
4,5 |
0,2 |
|
|
CO2 pro Türöffnung |
16 |
3,9 |
0,3 |
|
30 % O2 |
O2 pro Tag |
0,6 |
7,9 |
|
30 % O2 |
O2 pro Tag |
0,6 |
17,3 |
|
|
|
|
O2 pro Türöffnung |
19 |
10 |
0,8 |
|
|
O2 pro Türöffnung |
33 |
9 |
0,7 |
|
5 % O2 |
N2 pro Tag |
15 |
246 |
|
5 % O2 |
N2 pro Tag |
12 |
540 |
|
|
|
|
N2 pro Türöffnung |
173 |
147 |
9,2 |
|
|
N2 pro Türöffnung |
300 |
148 |
3,5 |
|
1 % O2 |
N2 pro Tag |
72 |
901 |
|
1 % O2 |
N2 pro Tag |
53 |
1972 |
|
|
|
|
N2 pro Türöffnung |
350 |
283 |
12,4 |
|
|
N2 pro Türöffnung |
640 |
405 |
8,2 |
|
0,2 % O2 |
N2 pro Tag |
125 |
1480 |
|
0,2 % O2 |
N2 pro Tag |
207 |
3712 |
|
|
|
|
N2 pro Türöffnung |
452 |
388 |
21,0 |
|
|
N2 pro Türöffnung |
929 |
677 |
13,9 |
Die Zahl unter break-even gibt im Prinzip an, ab wie vielen Türöffnungen pro Tag ein Inkubator mit geteilten Türen besser wäre. Je niedriger die Zahl, umso sinnvoller ist ein Brutschrank mit geteilten Türen. Hier zeigt sich deutlich, dass für Hypoxie fast immer ein Inkubator ohne Unterteilung besser ist.
Oberflächenmaterial
Ebenfalls wichtig für die Reinigbarkeit (nach DIN und GMP) ist das Material der Oberfläche. Hier gibt es:
+/- Kupferinnenraum und Einlegeböden (anti-bakteriell, aber schwer zu reinigen da es rau wird, teuer, nur für universitäre Forschung)
+ Edelstahl (gute Reinigbarkeit, da es sehr glatt ist, die Wahl für ATMP und TEMP sowie Testlabore)
++ Kupfer/Edelstahllegierungen (ebenfalls anti bakteriell, aber trotzdem gut zu reinigen, also die beste Variante; allerdings teurer, daher GMP Produktion oder ATMP nach Prüfung)
Wir haben wegen der Reinigbarkeit hier klar Edelstahl als Favoriten.
Reinigbarkeit der Oberflächen (Risiken und Aufwand)
|
Dies ist ein Kriterium welches oft übersehen wird, aber großes Potential hat. Denn sind wir mal ehrlich, wie viel Spaß macht es, das innere Gestänge eines Inkubators auseinander zu bauen und dann einzeln zu reinigen? Hier gilt ganz klar - je weniger je besser. Das liegt an zwei Punkten:
|
 |
Reinigbarkeit: Worauf sollte man also achten?
- Innenraum ohne Schweißnähte, d.h. aus einem Stück gezogen (ein MUSS für ATMP und TEMP)
- Abgerundete Ecken
- Türen ohne Schweißnähte
- Möglichst wenig Gestänge und Schrauben
- Leichte Demontage zur Reinigung (vor der Sterilisation: autoklavierter Schmutz ist eine Nährstoffquelle für neue Keime)
In unseren Augen die Nase vorn hat hier ganz klar Binder. Ihr Anti-Plenum Konzept ist bisher ungeschlagen, da der Inkubator gar kein Gestänge mehr hat, sondern nur noch die Einlegeböden. Auch der Eppendorf Inkubator ist mit einem sehr einfach und schnell zu demontierenden und zu reinigenden Gestell schon auf dem richtigen Weg.
Dekontaminations-Strategien Innenraum
Hier ist der Stand der Technik mittlerweile die automatische Dekontamination (sterile in place, SIP). Allerdings unterscheiden sich die Verfahren je nach Hersteller im Prinzip, der Temperatur und der Dauer:
|
Hitzesterilisation gemäß oder besser als in den Richtlinien wie DIN Normen und Arzneibüchern gefordert (für ATMP und TEMP) |
|
Dekontamination, aber keine normgemäße Sterilisation (ausreichend für Forschung und Assay-Labore) |
|
Bisher nur von Panasonic. Erscheint uns eher wenig sinnvoll, da beim Zerfall von H2O2 Wasser entsteht und somit alle Teile nach der Dekontamination nass sind. Allerdings ist H2O2 ein absoluter GMP Trend und könnte evtl. gegen sehr hartnäckige Keime bessere Ergebnisse erzielen. Dies gilt es aber noch zu belegen. |
Sterilisation: Vorgaben in Arzneibüchern und Normen
In Arzneibüchern wie den Pharmakopöen aus Europa, den USA, Japan etc. und den Normen zur Sterilisation werden die Begriffe Desinfektion und Sterilisation voneinander unterschieden. Desinfektion ist eine sogenannte Keimabreicherung also Verringerung der Keimzahl um 3-5 Zehnerpotenzen z.B. von 1.000.000 auf 10 Keime (5 Zehnerpotenzen). Entsprechend spricht man von Sterilisation erst, wenn keine Keime mehr nachweisbar sind. Dies wird bei einer Abreicherung um 6 Zehnerpotenzen als gegeben angenommen, also bei einer Reduktion von 1.000.000 auf 1. Je nach Vorgabe muss eine Desinfektion oder Sterilisation sichergestellt und validiert werden. In Inkubatoren wird trockene Hitze ohne Druck verwendet, dies unterscheidet sich von z.B. Autoklaven und daher sind auch andere Haltezeiten der Temperatur notwendig.
| Norm oder AB | Temperatur | Haltezeit |
| European Pharmacopoeia | 160 °C | 120 min |
| US Pharmacopoeia | 170 °C | 120 min |
|
DIN EN 556 |
160 °C 180 °C |
120 min 30 min |
Zusätzliche Dekontaminationsmechanismen (Luft)
Mehrere Anbieter statten ihre Inkubatoren mittlerweile mit HEPA-Filter (high efficiency particulate air) zur Filtration von CO2 und Luft aus. Obwohl durch die Türöffnung immer Keime in den Brutschrank gelangen, ist die Filtration der Gaszufuhr als risikominimierende Maßnahme positiv zu bewerten und damit eigentlich immer besser als keine Filtration. Allerdings müssen die Filter ausgetauscht werden, was Kontrolle erfordert und Geld kostet. In vielen Fällen muss jedoch bei Verwendung von Filtern ein Ventilator zur Verteilung genutzt werden. Dieser ist für uns aber ein wirkliches Kontaminationsrisiko. Daher würden wir diese Kombination ablehnen. Für ATMP und TEMP sollte man Filter in Betracht ziehen, jedoch nur ohne Ventilator. In anderen Laboren geht es sowieso ohne.
Steckdosen im Innenraum oder Kabelkanäle
|
Wer darüber nachdenkt neue Assays wie Impedanzmessungen mit dem xCelligence oder Live Cell Imaging mit z.B. dem Juli zu machen oder einen Schüttler im Inkubator braucht, der sollte auch daran denken, dass Kabeldurchführungen am Inkubator die Dichtigkeit enorm erhöhen. Diese sind normalerweise in der Seitenwand integriert und lassen sich nicht nachträglich installieren. Für Inkubatoren von Binder können - gegen Aufpreis - Durchführungen nach Kundenwunsch platziert werden. |
 |
Vibrationen (z.B. durch Ventilatoren oder Pumpen)
Ventilatoren und Pumpen können zu störenden Vibrationen im Inkubator führen. Diese sind absolut kontraproduktiv für Koloniebildungs-Assays, Stammzell- und andere Sphäroid-Kulturen und können außerdem das Adhärieren der Zellen in Multiwellplatten beeinflussen. Aus diesem Grund ist - unserer Meinung nach - von Ventilatoren im Brutschrank abzuraten. Da die Vibration nicht in der Baumusterprüfung nach DIN Norm getestet wird, sollte man beim Vergleich der Hersteller in Bezug hierauf spezifisch nachfragen.
Zusätzlich haben wir die Erfahrung gemacht, dass Brutschränke mit Ventilatoren öfter im Bereich der Ventilator-Verschraubung innerhalb der Decke verkeimen können. Besonders Pilze können sich dort ansiedeln. Wenn sie vorhanden sind, werden die Sporen durch den Ventilator zusätzlich leichter verwirbelt. Daher sehen wir Ventilatoren generell kritisch.
Evtl. O2-Regelung
Wer mit oxidativem Stress arbeitet, sollte sich schon jetzt überlegen, ob eine Sauerstoffregelung nicht sinnvoll ist. Die Hypoxie-Forschung folgt hier nämlich - wenn auch sehr langsam - dem Trend anzuerkennen, dass ein physiologischer Sauerstoffgehalt deutlich unter dem von Luft und damit den 21% im Inkubator liegt.
Qualifizierung und Validierung: Serviceleistungen
In GMP und GLP Laboren, also auch in solchen, die ATMP und TEMP herstellen, müssen Geräte qualifiziert werden. D.h. bei einem Neukauf muss gemäß QbD (quality by design) ein Lasten- und Pflichtenheft erstellt werden und nach dem Kauf muss das Gerät im Labor am vorgesehenen Platz qualifiziert werden. Die Qualifizierung umfasst somit DQ, IQ, OQ und PQ (design qualification, installation qualification, operational qualification und performance qualification). Der ganze Prozess ist aufwendig und erfordert eine detaillierte Dokumentation. Er kann gemäß eines eigenen Validierungsplans durchgeführt werden, aber manchmal ist es sinnvoll und deutlich schneller, wenn man hierfür einen Service des Herstellers in Anspruch nimmt. Die Qualifizierungsdokumentation für einen Inkubator kann ca. die Dicke eines Leitzordners umfassen.
Hersteller-Vergleich und Übersicht zu den Inkubatoren
Im Folgenden haben wir einen Vergleich der Hersteller und eine Übersicht über die uns vorliegenden technischen Daten zusammengestellt.
Eppendorf (ehemals New Brunswick Inkubatoren)
 |
|
| Produktionsorte | Deutschland |
| QMS | ISO9001:2008 |
| Model | CellXpert C170 / C170i (170 L, Nachfolgemodel des Galaxy) |
| Kontaminationsvermeidung |
|
| Ventilator | + Nein. |
| Vibrationen | + Nein bis wenig, da kein Lüfter/Ventilator. |
| Mantel |
Lüfterlose Direktbeheizung aller 6 Kammerseiten. Kondensationsfalle in Wasserwanne durch eigenen Heizkreis. |
| Türheizung | Ja. |
|
Oberflächen (GMP-relevant)
|
Innenraum nahtlos aus einem Stück Edelstahl ausgezogen, keine Schweißnähte, wenige Einbauten in ca. 40 s zu demontieren. Kupferkammer als Option möglich. |
Anzahl Türen (indirekt GMP-relevant) |
1, 2, 4, 8 (je nach Modell). |
| Türscharniere | Stabil über die gesamte Höhe der Türen bei neuen Geräten. Anschlagsseite nachträglich wechselbar. |
| Erholungszeit T (GMP-relevant) |
< 5 min(30s Türöffnung). |
| Temperatur-Bereich |
4°C über RT bis 50°C. Mehrere Temperatursensoren. |
Temperatur-Schwankungen |
Abweichung von 37°C: +/- 0,1K Mess-Genauigkeit, +/- 0,3K Schwankung in der Homogenität. Messung nach DIN12880. |
Feuchte-System (GMP-relevant) |
Herausnehmbare Wanne mit Konsensationsfalle (eigener Heizkreis). Feuchteüberwachung optional. |
| CO2 -Zugabe | |
|
CO2 -Erholung (GMP-relevant)
|
< 5 min (30s Türöffnung). |
| Sterilisation (GMP-relevant) | Je nach Modell 140 – 180°C automatische Desinfektion mit downloadbarem Protokoll. |
| Sterilisations-Dauer (indirekt GMP-relevant) | Inkl. Aufheizen, Sterilisation, Abkühlung: 14h. |
| Sensoren (GMP-relevant) | Zwei-Kanal Infrarot-Sensor für CO2, wartungsarm. Alle Sensoren sind sterilisierbar und können bei der Dekontamination im Gerät bleiben. |
| Sensoren-Platzierung | Oben-Mitte. Daher genauere bzw. realistischere Messung des CO2-Gehalts. |
| HEPA-Filter (indirekt GMP-relevant) | Ja, in den Gasschläuchen. |
| Datenlogger (indirekt GMP-relevant) | VisioNize® Software mit solid state Festplatte zur langfristigen Speicherung, 2x USB, Ethernet-Schnittstelle. |
| Validierungs-Hilfen (GMP-relevant) | IQ/OQ bestellbar. |
| Kabel und Steckdosen | 2 Kabeldurchführungen bereits vorhanden. |
| Sauerstoff | Optional. |
| Energieverbrauch | 100W bei 37°C. |
| Preisniveau | Mittel bis hoch. |
| Bekannte Vorteile |
|
| Bekannte Nachteile |
|
| Weitere Informationen | |
| Webseite | Produkte |
Binder
 |
|
| Produktionsorte | Deutschland |
| QMS | ISO9001:2008 |
| Ventilator | + Nein |
| Vibrationen | |
| Mantel |
Luftmantelsystem, Kondensationsfalle in der Wasserwanne. |
| Türheizung | |
|
Oberflächen (GMP relevant)
|
Innenraum aus ausgezogenem Edelstahl, keine Schweißnähte, keine Einbauten außer den Blechen. |
|
Anzahl Türen (indirekt GMP relevant)
|
1, 4 |
| Türscharniere | Stabil aber nicht über die gesamte Höhe der Türen. |
| Erholungszeit T (GMP relevant) | Schnelle Temperaturerholung: 4min (bei 30s Öffnung; neue DIN12880) |
| Temperatur-Bereich | 5-7°C über RT bis 60°C |
| Temperatur-Schwankungen | Abweichung von 37°C: +/- 0,3K |
|
Feuchte-System
|
Herausnehmbare Wanne mit spezieller Kältefalle, damit Wasser nur unten kondensiert und nicht an Türen oder Wänden. Feuchte 90-95%. |
| CO2 -Zugabe | Zugabe nach homogener Mischung mit Luft über ein spezielles Ventil. |
| CO2 -Erholung | Schnell: 7min (bei 30s Öffnung; neue DIN12880) |
| Sterilisation | Automatische Sterilisation gemäß oder über Arzneibuch und Normanforderungen. 180°C, 120 min |
| Sterilisations-Dauer | Inkl. Aufheizen, Sterilisation, Abkühlung: 10h |
| Sensoren | Infrarot-Sensor für CO2, wartungsarm. Alle Sensoren sind sterilisierbar. |
| Sensoren-Platzierung | Oben. Daher genauere bzw. realistischere Messung des CO2-Gehalts. |
| HEPA-Filter | Nein |
| Datenlogger | Ethernet-Schnittstelle zur Anbindung an einen Computer mit der Binder Software Apt.com. |
| Validierungs-Hilfen | Ja. Voller IQ, OQ Support mit Dokumentations-Vorlagen gegen Aufpreis. |
|
Kabel und Steckdosen
|
Kabeldurchführungen können gegen Aufpreis integriert werden. Auf Kundenwunsch auch an besonderen Stellen. |
| Sauerstoff | Möglich |
| Energieverbrauch | 100W |
| Preisniveau | Mittel bis hoch |
| Bekannte Vorteile |
|
| Bekannte Nachteile | |
| Weitere Informationen |
Weiterführende Informationen im Downloadcenter: https://www.binder-world.com/de/download-center. Wir haben das Vorgängermodell, den CB150, für einige Tage getestet und waren sehr zufrieden. Absolut überrascht hat uns die Spedition, die das Leihgerät geliefert hat. Der Mitarbeiter fährt nur Binder Geräte aus, bringt sie ins Labor und baut sie dort komplett auf. Kein Ärger, keine Hektik, kein bis Hierhin und nicht weiter - das war super! Die Inneneinbauten sind wirklich gut durchdacht und gelungen. Wie versprochen konnten wir keine Kondensation im Innenraum feststellen. Die Türen sind stabil und besonders die Außentür mit Griff verhindert, dass der Inkubator versehentlich offen gelassen wird. |
| Webseite | Produkte |
Bioair S.p.A. Tecnilabo - Cellcare Inkubatoren
 |
|
|
Produktionsorte |
Italien |
|
QMS |
EN12469:2000 |
|
Ventilator |
Nein |
|
Vibrationen |
Anti-Vibrations Tür |
|
Mantel |
Glatte Flächen, mit lackiertem Stahl, keine Ventilatoren oder HEPA-Filter |
|
Türheizung |
Nein |
|
Oberflächen |
4 Edelstahl Tablare & Wasserbad, entnehmbar und autoklavierbar, gezogener Innenraum |
|
Anzahl Türen |
1 (Verfügbar optional mit einzelnen Innentüren) |
|
Türscharniere |
Antivibrations-Türen, leicht zu verschließen, (optional mit automatischer Schließfunktion |
|
Erholungszeit T |
CO2 und Temperatur Erholzeit unter 5 Minuten |
|
Temperatur-Bereich |
5°C über RT bis 50°C. Kann der Inkubator auch kühlen? Nein! |
|
Temperatur-Schwankungen |
|
|
Feuchte-System |
Herausnehmbare Wasserbadschale aus Edelstahl (siehe oben) |
|
CO2 -Zugabe |
Besondere Steuerung ? Nein |
|
CO2 -Erholung |
CO2 Erholzeit unter 5 Minuten |
|
Sensoren |
Multiparameter Sensoren (IR Sensor) |
|
Sterilisation |
180°C Decontaminationsprogramm |
|
Sterilisations-Dauer |
Bitte frage sende ein Mail an Eugenio von BioAir |
|
Sensoren-Platzierung |
Bitte frage Eugenio |
|
HEPA-Filter |
Nein |
|
Datenlogger |
Ja, Echtzeit Datenspeicherung, Touchdisplay mit USB und Ethernet Schnittstellen |
|
Validierungs-Hilfen |
IQ/OQ/PQ Ja ist möglich über unsere Service Abteilung sep. Artikelnummer |
|
Kabeldurchführung und Steckdosen |
Ja ist vorhanden… |
|
Sauerstoff |
O2 Begasung ist Optional bestellbar mit Aufpreis |
|
Energieverbrauch |
Z.B. 100W bei 37°C. Bitte Eugenio fragen von BioAir |
|
Preisniveau |
Listenpreis mit Modelbeschreibung oder grobe Einordnung: z.B. mittel bis hoch. Bitte frage dazu Emanuele |
|
Bekannte Vorteile |
|
|
Bekannte Nachteile |
|
|
Weitere Informationen |
Made in the EU |
|
Webseite |
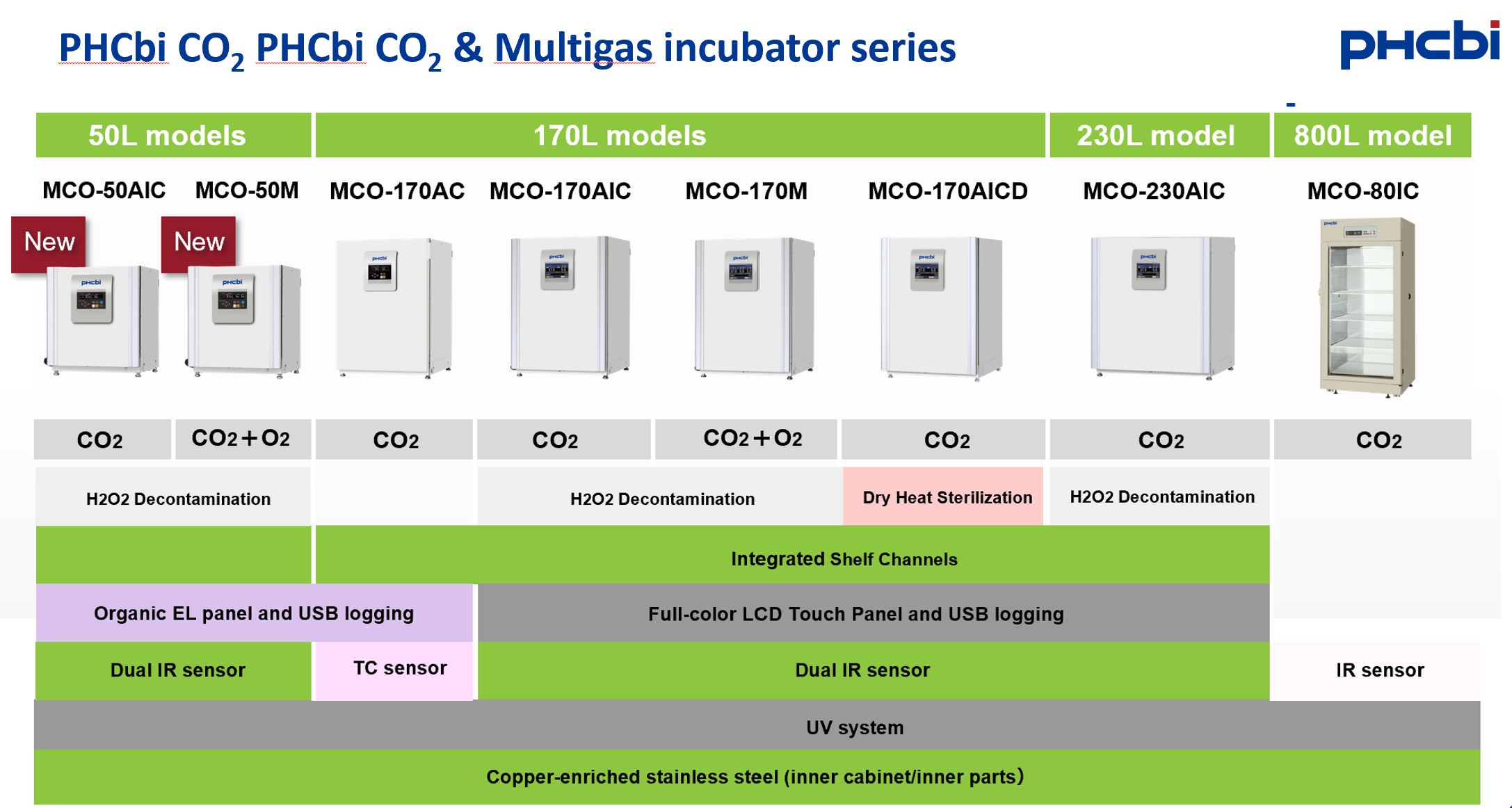
PHCbi (ehemals Panasonic, Sanyo)
 |
 |
|
Produktionsort |
Herstellung vollständig in Indonesien. Design aus Japan. |
|
QMS |
ISO 9001:2015, ISO 140001:2015 and ISO 13485:2016. Medizinprodukt-Zertifizierung. MCO-170AIC-PE, MCO-170AICD-PE, MCO-230AIC-PE, MCO-170M-PE Serien zertifiziert als Klasse IIa Medizinprodukt (93/42/EEC and 2007/47/EC) für medizinische Anwendungen wir Kultivierung von Zellen, Gewebe, Organen (ATMP, TEMP, Stammzellen, Gewebezubereitungen) und befruchteten Eizellen (Embryos) für die künstliche Befruchtung. |
|
Kontaminations-Vermeidung (GMP-relevant)
|
|
|
Ventilator |
Ja, aber hier keine bekannten Kontaminationsprobleme (evtl. durch das UV Licht) |
|
Vibrationen |
Keine Angaben. |
|
Mantel (Gehäuse) |
Alle CO2 und Multigas-Inkubatoren haben ein air jacket (Luftmantel), außer die MCO-170AICD-PE (Hitze-Sterilisierung) Serie. Die MCO-170AICD Reihe hat eine Melamin-Schaum Isolierung, diese sichert eine hohe thermische Isolierung und exzellente Hitzebeständigkeit. Diese Melamin-Schaum Isolierung limitiert die Hitzeabgabe bei der Sterilisation durch trockene Hitze. Hierdurch können Zellen in benachbarten Inkubatoren unbeeinflusst weiterwachsen während in Inkubatorstapel der MCO-170AICD dekontaminiert wird. |
| Türheizung |
Ja. Alle CO2 und Multigas-Inkubatoren haben eine Türheizung als Teil ihres Direktheizsystems. Dieses System reguliert die Temperatur durch 3 unabhängige Heizzonen die durch Microprocessor P.I.D. Kontrolle geregelt werden. (P.I.D.: Proportional Integral Derivative) |
|
Oberflächen (GMP-relevant)
|
Alle internen Oberflächen bestehen aus mit Kupfer angereichertem Edelstahl (InCusaFe®). Hierdurch ist die Oberfläche anti-bakteriell, bleibt aber leicht zu reinigen. Die Reinigbarkeit wird weiterhin durch die abgerundeten Ecken und integrierten Bodenhalterungen erhöht. Alle inneren Komponenten einschließlich des belüftungsfördernden Plenums, der Wasserwanne und des ventilators sind ohne Werkzeuge leicht herauszunehmen wenn nötig. Wenn Komponenten herausgenommen werden, sind alle internen Oberflächen zugänglich für eine einfaches Reinigen mit Tüchern und Desinfektionsmitteln. Integriertes Selbsthaltesystem für Einlegeböden zur einfachen Reinigung erhältlich für MCO-170AC-PE, MCO-170AIC-PE, MCO-170AICD-PE, MCO-170M-PE and MCO-230AIC-PE Serien. |
|
Geteilte Türen (indirek GMP-relevant)
|
Alle Brutschränke haben 1 äußere und 1 innere, ungeteilte Tür, außer MCO-170M-PE Multigas und MCO-170AIC-PE Serien. Geteilte Türen gibt es als innere Standardedelstahltür mit 4 Glastüren für die MCO-170M-PE Multigas Serie und diese Option ist auch als Option für die MCO-170AIC-PE Serie erhältlich. |
|
Türscharniere |
Die äußeren und inneren Türen sind als Standard links angeschlagen, sind aber auch rechts anschlagbar. Die Türdichtungen sind magnetisch, um die Gasleckage zu reduzieren. |
| Türen abschließbar (indirekt GMP relevant) |
Elektronisches Türschloss mit Passwortschutz ist als Standardausstattung erhältlich für die MCO-170AICUVH-PE, MCO-170MUVH-PE, MCO-230AICUVH-PE, MCO-170AICD-PE und MCO-170AICUVD-PE Reihen. Das set up ist sehr einfach. Andere MCO-170AIC-PE, MCO-170AICD-PE, MCO-170M-PE and MCO-230AIC-PE Serien sind kompatibel mit einem optionalen Türschloss (MCO-170EL). |
|
Erholzeit T (GMP-relevant) |
Temperatur-Erholzeiten werden nicht nach DIN12880 getestet. Erholzeiten sind in allen Produktbroschüren angegeben.Sie variieren je nach Model. |
| Temperaturbereich |
Nutzbar in Bereich von +5°C to 50°C. Die CO2 und Multigas-Inkubatoren haben keine Kühlfunktion. Ein Überhitzungsschutz ist einstellbar und eine Standardausstattung. |
|
Temperatur Abweichungen (GMP-relevant) |
Direktheizer und Luftmantel haben ein Heizsystem mit P.I.D Temperaturkontrolle; Variation +/- 0.1°C. Temperatur Homogenität ist +/- 0.25K. Test Konditionen: Raumtemperatur 23°C, Einstellung: 37°C, CO2 5%, O2 5%, unbeladen.Vgl. Spezifikationen in den Produktbroschüren. |
|
Feuchtesystem (GMP-relevant) |
Keine aktive Feuchte. Alle Brutschränke haben eine Wasserwanne, die leicht befüllt, gereingt und entnommen werden kann. Die Feuchteerholung ist jedoch gegenüber anderen Brutschränken, die nur eine Wanne haben besser, das durch den Ventilator kontinuierlich Luft über die Wanne geströmt wird. Die Bodenheizung kann separat durch einen Techniker reguliert werden, um die RH% höher oder niedriger einzustellen. Feuchtegehalt und Schwankungen: RH% ist 95% +/- 5%. Kondensations-Management mit einem ‘dew stick’ der über Peltier Technologie geregelt wird - er kondensiert Wasser auf seiner Oberfläche, das dann in die Wasserwanne tropft. Dies verhindert ungewollte Kondensation in der Inkubatorkammer und damit die Kontamination des Schranks. |
|
CO2 Versorgung |
Einströmendes CO2 wird durch einen HEPA Filter filtriert bevor es in den Brutschrank eingeströmt. CO2 kann auf 0.03 MPa(G)–0.1 MPa(G) eingestellt werden. (Empfohlener Druck: 0.03 MPa(G)). CO2 Schläuche werden als Standard mitgeliefert. |
|
CO2 Erholung (GMP-relevant) |
CO2 - Erholzeiten werden nicht nach DIN12880 getestet. Erholzeiten sind in allen Produktbroschüren angegeben.Sie variieren je nach Model. |
|
Sensoren (indirekt GMP-relevant) |
Alle MCO-170 und MCO-230 Serien haben Temperatur- und Feuchte-geschützte (state-of-the-art, Stand von Wissenschaft und Technik, schneller) IR CO2 -Sensoren - Einzelstrahl mit Dualsensor für kontinuierliches Auto-zeroing, um die CO2 -Präzision zu gewährleisten. Die P.I.D CO2-Kontrolle stellt eine schnelle Erholzeit auf den CO2 set-point sicher. CO2 Bereich: 0 to 20 %, Variation +/-0.15 % 37°C und 5 % Gehalt. MCO-5AC-PE, MCO-5M-PE and MCO-170AC-PE haben TC Sensoren. Alle können während der H2O2-Dekontamination oder der Hitzesterilisation in ihrer Original position verbleiben. Eine Kalibration nach der Dekontamination ist nicht notwendig. Dual IR CO2 Sensor- Einzelstrahl mit Dualsensor für kontinuierliches Auto-zeroing, um die CO2 -Präzision zu gewährleisten. Sensoren sind Temperatur- und Feuchte-geschützt: MCO-170AC-PE, MCO-170AIC-PE, MCO-170AICD-PE, MCO-170M-PE and MCO-230AIC-PE series. Solid State Zirconia O2- Sensor mit P.I.D Kontrolle für eine schnelle Erholung des O2 set-point in MCO-170M-PE und MCO-5M-PE Serien. |
|
Sterilisation (GMP-relevant)
|
Hitzesterilisation: Der eigentlich Sterilisationsprozess beginnt, sobald die innere Kammer 180°C erreicht hat und läuft dann 60 min. Nachfolgend erfolgt passive die Abkühlung. H2O2 Dekontamination: vollständiger Zyklus in 3 Stunden. Das ist die schnellste Dekontaminationsmethode auf dem Inkubatormarkt. Vgl. Daten in den Broschüren. |
|
Dauer der Sterilisation (indirekt GMP-relevant) |
Hitzesterilisation: Gesamtzyklus in 11 h. H2O2 Dekontamination: Gesamtzyklus in 3 h. |
|
Sensorposition |
Der Sensor sitze in einer Sensorbox im hinteren teil des Brutschranks. Die Öffnung des Sensors ist im Luftkanal positioniert. |
|
HEPA filter (indirekt GMP-relevant) |
Ja, für zugeführtes CO2, O2 und N2 Gas. |
|
Datenlogger (indirekt GMP-relevant) |
Als Standard haben die MCO-170 und MCO-230 Serien alle einen USB Port für das Logging von Temperatur, CO2, Türöffnungsstatus und Alarmen. Der Standard-USB-Port erlaubt einen bequemen Datentransfer über einen USB Stick auf einen Computer. Daten werden ca. 1.5 Monate gespeichert, wenn ein 2-Minuteninterval gewählt wird. (Einstellbarer Bereich: 2~30 min.) Optionales analoges Interface (4-20mA) ist erhältlich. |
|
Validierungs-Support (GMP-relevant) |
IQ/OQ wird angeboten. Preis auf Nachfrage. |
|
Kabeldurchführungen und Steckdosen |
Ein 30mm Zugangsport / Durchführung ist standardmäßig in jedem Inkubator verbaut. |
|
Sauerstoff |
Ja, heißt bei PHCbi Multigas Inkubator: Standard für MCO-170M-PE und MCO-5M-PE Serien. |
|
Energieverbrauch |
Z.B. 100 W bei 37°C. Abhängig vom Model. Daten auf Nachfrage. |
| Stapelbar |
Inkubatoren können mit optionalem "stacking kit" gestapelt werden. |
|
Price range |
Variiert mit den Modellen. Information auf Nachfrage erhältlich. Kostengünstigeres Model verfügbar. |
|
Bekannte Vorteile |
|
|
Weitere Informationen |
Service and download Seite für weitere Informationen. |
|
Website |
Produktseite incubators. |
Memmert
 |
 |
| Produktionsorte | Deutschland |
| QMS | ISO9001:2008 / 12880:2007-05. Ein Inkubator ist als Medizinprodukt Kl. IIa zugelassen: ICOmed. |
| Ventilator | + Nein |
| Vibrationen | Ein Kühl-Brutschrank ohne Kompressor und stattdessen mit Peltierelement ist als besonders vibrationsfrei ausgewiesen. |
| Mantel |
Luftmantel. Keramikmetall-ummantelte Großflächenheizung. |
| Türheizung | Ja. |
|
Oberflächen
|
Tiefgezogen, fugenlos verschweißt. |
|
Anzahl Türen
|
1, 2 oder mehrere je nach Modell bestellbar. |
| Türscharniere | 2-Punkt-Verriegelung (Kompressions-Türverschluß). |
| Erholungszeit T |
Schnelle Temperaturerholung bei 37 °C (30 Sekunden Tür geöffnet) variiert zwischen den verschiedenen Modellen: 50 = 3 min 105 = 4 min 150 = 5 min 240 = 6 min Nach DIN12880:2007-05. |
| Temperatur-Bereich | +18 bis +50 °C. |
| Temperatur-Schwankungen | Abweichung von 37°C: +/- 0,1K. |
|
Feuchte-System
|
93 % rh +/- 2,5 % (relative Feuchte). Feuchtebegrenzung durch Peltier-Element. Integrierte Feuchtebegrenzungsregelung. |
| CO2 -Zugabe | Geräterückseite. |
| CO2 -Erholung |
Im 5 % CO2 Brutschrank (30 Sekunden Tür geöffnet): 50 = 6 min 105 = 6 min 150 = 7 min 240 = 7 min Nach DIN12880:2007-05. |
| Sterilisation | Sterilisation nach DIN Norm. |
| Sterilisations-Dauer | Hinterlegtes Sterilisationsprogramm: 60 Minuten bei 180 °C, Abkühlzeit nicht angegeben. |
| Sensoren | 2 Pt100-Sensoren DIN-Klasse A in 4-Leiter- Messung mit wechselseitiger Überwachung und Funktionsübernahme bei exakt gleichem Temperaturwert. |
| Sensoren-Platzierung |
Temperaturfühler: Rückwand hinten, oben links. CO2-Fühler: Rückwand hinten, halbe bis 2/3 Gerätehöhe links (je nach Gerätegröße). Feuchtefühler: ähnliche Position wie CO2-Fühler. O2-Fühler: Rückwand hinten, halbe bis 2/3 Gerätehöhe rechts (je nach Gerätegröße). |
| HEPA-Filter | Ja, Innenraum. |
| Datenlogger | AtmoControl Software, USB Schnittstelle, Ethernet-Schnittstelle. |
| Validierungs-Hilfen | IQ/OQ/PQ bestellbar. |
|
Kabel und Steckdosen
|
Silikondurchführung. |
| Sauerstoff | Ja, optional. |
| Energieverbrauch |
50 = 60 W bei 37 °C 105 = 60 W 150 = 80 W 240 = 85 W |
| Preisniveau | Mittel bis hoch. |
| Bekannte Vorteile |
|
| Bekannte Nachteile | |
| Weitere Informationen | Produktinformation und Broschüren können im Downloadbereich herunter geladen werden. |
| Webseite | Produkte |
Weitere Hersteller von Zellkultur Inkubatoren sind
Hettich (Produkte; dieser Inkubator wird 2015 gelauncht), Memmert (Inkubatoren), PHCbi vorher Panasonic (Inkubatoren), Thermo Fischer (Inkubatoren, Heraeus), Dunn Labortechnik (Inkubatoren), NuAir vertrieben durch IBS Integra Technomara (Inkubatoren), Ewald Innovationstechnik (Inkubatoren), Infors AG (Inkubatoren), Labotec GmbH (Inkubatoren), Selutec GmbH (Inkubatoren).
Kaufkriterien Inkubatoren für Forschungslabore
Natürlich ist in allen Laboren der Preis immer ein wichtiges Kriterium. Trotzdem sollte man sich das Leben nicht unnötig schwer machen, nur um ein bisschen Geld zu sparen. Für uns gilt also folgende Wertigkeit im Forschungslabor:
- kein Ventilator außer er ist gut zu reinigen und verpilzt nicht (Kein Thermoinkubator!, Panasonic hat das Problem nicht.)
- geteilte Türen, gute Scharniere
- Wasserwanne
- möglichst wenig Gestänge im Innenraum, möglichst ausgezogener Innenraum
- Erholzeiten so kurz wie möglich (Temperatur, Feuchte, CO2)
- schnelle CO2 Erholung nach Türöffnung
- Preis
- Datenlogger ohne PC zur Kontrolle der Wachstumsbedingungen und Türöffnungen
- Hitzesterilisation
Kaufkriterien Inkubatoren für Pharma-QK Testlabore (Potency Assays, Freigabeassays)
Hier kommt es auf die Konstanz, Reproduzierbarkeit und Variabilität der Daten an. Außerdem arbeiten die meisten Testlabore nach einer ISO oder unter GMP/GLP. Daher haben wir hier folgende Präferenzreihenfolge für den Herstellervergleich:
- kein Ventilator außer er ist gut zu reinigen und verpilzt nicht (Kein Thermoinkubator!, Panasonic hat das Problem nicht.)
- geteilte Türen, gute Scharniere (wenn Türen häufig geöffnet werden)
- Wasserwanne oder Verdampfer
- Erholzeiten so kurz wie möglich (Temperatur, Feuchte, CO2)
- Datenlogger möglichst mit Schnittstelle und Software zur Kontrolle der Wachstumsbedingungen und Türöffnungen
- möglichst wenig Gestänge im Innenraum, möglichst ausgezogener Innenraum
- Kabeldurchführungen
- eher zwei kleine als ein großer Inkubator um die Türöffnungen zu verringern
- schnelle CO2 Erholung nach Türöffnung
- Preis
- Hitzesterilisation bei 180°C für 2 Stunden
Kaufkriterien Inkubatoren für ATMP und TEMP Hersteller
ATMP und TEMP sind Arzneimittel, d.h. sie unterliegen strengen Kontrollen und müssen qualitativ hochwertig sein. Außerdem müssen sie Vorgaben erfüllen und die technische Ausstattung zur Herstellung muss dem Stand der Technik entsprechen. Daher gibt es hier ein paar Punkte, die ein absolutes MUSS darstellen.
- kein Ventilator außer er ist gut zu reinigen und verpilzt nicht (Kein Thermoinkubator!, Panasonic hat das Problem nicht.)
- Inkubator ist als Medizinprodukt unter ISO13485 hergestellt (Vergleich mit Risikoanalyse anderer Inkubatoren) ist ein sehr starkes Kriterium, das gegen andere abgewogen werden sollte, da es nicht viel Inkubatoren gibt, die dieses Kriterium erfüllen
- Hitzesterilisation bei 180°C für 2 Stunden (Stand der Technik gefordert, SIP)
- keine Kupferoberfläche (Reinigbarkeit gefordert)
- möglichst wenig Gestänge im Innenraum, möglichst ausgezogener Innenraum (Reinigbarkeit gefordert)
- Erholzeiten so kurz wie möglich (Temperatur, Feuchte, CO2)(gleichbleibende Qualität, Abweichungen vom Soll müssen begründet und bewertet werden)
- Datenlogger möglichst mit Schnittstelle und Software zur Kontrolle der Wachstumsbedingungen und Türöffnungen (Stand der Technik, ansonsten manuelle Kontrolle und Dokumentation mindestens täglich)
- DIN-konforme Steuerung und Nutzerverwaltung mit Code
- eher zwei kleine als ein großer Inkubator um die Türöffnungen zu verringern (Risiko-minimierende Maßnahme, Variabilität)
- Wasserwanne oder Verdampfer (letzteres wäre u.U. als sicherer anzusehen, muss bewertet werden, QbD)
- Ersatzflasche für CO2